Wykres topnienia i krzepnięcia wody to jeden z najbardziej fundamentalnych i pouczających diagramów w fizyce, który w przystępny sposób ilustruje procesy przemian fazowych. Jego zrozumienie jest kluczowe dla każdego, kto chce zgłębić podstawy termodynamiki i zrozumieć zjawiska zachodzące w otaczającym nas świecie, od zamarzających jezior po działanie systemów chłodniczych. To modelowy przykład przemiany fazowej pierwszego rodzaju, stanowiący nieodłączny element edukacji fizycznej.
Wykres topnienia i krzepnięcia wody: stała temperatura 0°C to klucz do zrozumienia fizyki
- Najważniejszym elementem wykresu jest stała temperatura 0°C podczas topnienia lodu i krzepnięcia wody, mimo dostarczania lub odbierania energii.
- Dostarczana lub odbierana energia w tym czasie jest zużywana wyłącznie na zmianę stanu skupienia (ciepło utajone), a nie na zmianę temperatury.
- Wykres składa się z odcinków skośnych (zmiana temperatury lodu/wody) oraz poziomych (przemiana fazowa w 0°C).
- Ciepło utajone topnienia wody jest bardzo wysokie, wynosząc około 333,7 kJ/kg, co świadczy o dużej ilości energii potrzebnej do stopienia lodu.
- Woda wykazuje anomalną rozszerzalność cieplną (największa gęstość w 4°C) oraz zjawisko przechłodzenia, gdzie może pozostać ciekła poniżej 0°C.
Zrozumienie wykresu topnienia i krzepnięcia wody
Dla mnie, jako fizyka, wykres topnienia i krzepnięcia wody jest niczym alfabet w nauce o materii. To nie tylko suchy diagram, ale przede wszystkim fundamentalne narzędzie do zrozumienia, jak energia wpływa na stan skupienia substancji. W polskiej edukacji fizycznej, zarówno na poziomie podstawowym, jak i średnim, jest to temat obowiązkowy, który często pojawia się na egzaminach i testach, służąc jako modelowy przykład przemiany fazowej pierwszego rodzaju.
Zrozumienie tego wykresu pozwala nie tylko zdać egzamin, ale przede wszystkim rozwija intuicję fizyczną. Uczy nas, że nie zawsze dostarczanie energii musi skutkować wzrostem temperatury, a także pokazuje, jak subtelne procesy zachodzą na poziomie molekularnym, gdy lód zamienia się w wodę lub odwrotnie. To esencja termodynamiki w pigułce.
Przeczytaj również: Transformator buczy? Odkryj, jak działa i co oznacza ten dźwięk
Jak krok po kroku odczytać wykres przemian fazowych wody
Wykres topnienia i krzepnięcia wody, choć na pierwszy rzut oka może wydawać się skomplikowany, w rzeczywistości jest bardzo logiczny. Składa się z charakterystycznych odcinków: skośnych i poziomych. Każdy z nich reprezentuje inny etap procesu, a ich interpretacja pozwala nam śledzić, co dzieje się z wodą (lub lodem) w miarę dostarczania lub odbierania energii.
Etap 1: Ogrzewanie lodu co dzieje się przed punktem zero?
Wyobraźmy sobie kostkę lodu wyjętą z zamrażarki, powiedzmy o temperaturze -10°C. Kiedy zaczynamy dostarczać jej energię, na przykład umieszczając ją w cieplejszym otoczeniu, na wykresie obserwujemy pierwszy, skośny odcinek. W tym etapie energia jest pochłaniana przez lód, a jego temperatura stopniowo wzrasta, aż osiągnie 0°C. Lód pozostaje lodem, zmienia się tylko jego temperatura.
Etap 2: Magia stałej temperatury, czyli samo serce procesu topnienia
To jest moment, który często zaskakuje osoby po raz pierwszy analizujące ten wykres i to jest jego najważniejszy punkt! Gdy lód osiągnie 0°C, mimo dalszego dostarczania energii, jego temperatura przestaje rosnąć. Na wykresie widzimy poziomy odcinek. Dlaczego? Cała dostarczana energia, nazywana ciepłem utajonym topnienia, jest zużywana wyłącznie na rozerwanie wiązań w strukturze krystalicznej lodu i przekształcenie go w wodę. Mamy tu do czynienia ze współistnieniem fazy stałej i ciekłej w stałej temperaturze 0°C.
Etap 3: Co dalej? Ogrzewanie wody, która już nie jest lodem
Gdy ostatnia cząsteczka lodu przekształci się w wodę, czyli cały lód stopi się, wykres ponownie zmienia swój charakter. Dostarczana energia zaczyna teraz ogrzewać powstałą ciekłą wodę. Obserwujemy kolejny skośny odcinek, tym razem w górę, gdzie temperatura wody wzrasta powyżej 0°C. Im więcej energii dostarczymy, tym wyższa będzie temperatura wody, aż do momentu, gdy zacznie ona wrzeć (co jest już kolejną przemianą fazową).
Od ciepła do zimna: analiza wykresu krzepnięcia wody
Proces krzepnięcia wody jest lustrzanym odbiciem topnienia. Zamiast dostarczać energię, musimy ją odbierać. To tak, jakbyśmy odwrócili film z topniejącą kostką lodu. Na wykresie obserwujemy te same etapy, ale w odwrotnej kolejności i z przeciwnym kierunkiem zmian temperatury.
Odbieranie energii: Jak woda przygotowuje się do zamarzania?
Zaczynamy od ciekłej wody, powiedzmy o temperaturze pokojowej. Kiedy zaczynamy ją oziębiać, czyli odbierać od niej energię, jej temperatura spada. Na wykresie odpowiada to skośnemu odcinkowi w dół, aż woda osiągnie temperaturę 0°C. W tym etapie woda pozostaje w stanie ciekłym, ale jej cząsteczki tracą energię kinetyczną, co objawia się spadkiem temperatury.
Kluczowy moment: Proces krzepnięcia w stałej temperaturze 0°C
Podobnie jak przy topnieniu, gdy woda osiągnie 0°C, jej temperatura przestaje spadać, mimo dalszego odbierania energii. Na wykresie pojawia się poziomy odcinek. W tym momencie woda zaczyna zamarzać, a energia, którą odbieramy, to ciepło utajone krzepnięcia, które jest uwalniane do otoczenia, gdy cząsteczki wody układają się w strukturę krystaliczną lodu. To kluczowy etap, gdzie współistnieją obie fazy: ciekła i stała.
Co dzieje się z lodem, gdy temperatura spada poniżej zera?
Po tym, jak cała woda zamarznie i przekształci się w lód, dalsze odbieranie energii powoduje spadek temperatury lodu poniżej 0°C. Widzimy to jako ostatni skośny odcinek wykresu, skierowany w dół. Lód staje się coraz zimniejszy, a jego temperatura może spadać znacznie poniżej zera, w zależności od ilości odebranej energii.
Tajemnice ukryte w wykresie: kluczowe pojęcia i zjawiska
Wykres topnienia i krzepnięcia wody to nie tylko sekwencja zmian temperatury i stanu skupienia. To także brama do zrozumienia głębszych zjawisk fizycznych, które mają ogromne znaczenie dla otaczającego nas świata.
Ciepło utajone topnienia: Dlaczego potrzeba tak dużo energii, by stopić lód?
Jak już wspomniałem, ciepło utajone topnienia to energia potrzebna do zmiany stanu skupienia bez zmiany temperatury. Dla wody jest ono niezwykle wysokie i wynosi około 333,7 kJ/kg. Aby to sobie uzmysłowić, pomyślmy o tym tak: do stopienia 1 kg lodu o temperaturze 0°C potrzeba tyle samo energii, co do ogrzania 1 kg wody o prawie 80°C! To pokazuje, jak silne są wiązania między cząsteczkami w strukturze lodu i jak wiele energii trzeba dostarczyć, aby je rozerwać. Ta właściwość ma ogromne znaczenie, na przykład w regulacji klimatu czy w systemach chłodniczych.
Rola ciśnienia: Jak zmiana warunków wpływa na temperaturę topnienia?
Większość substancji pod wpływem wzrostu ciśnienia zwiększa swoją temperaturę topnienia. Woda jest tutaj wyjątkiem, czyli wykazuje anomalię. Wzrost ciśnienia nieznacznie obniża jej temperaturę topnienia i krzepnięcia. Dlaczego? Odpowiedź tkwi w strukturze lodu. Lód ma mniejszą gęstość niż woda (dlatego pływa!), co oznacza, że zajmuje większą objętość. Zwiększenie ciśnienia sprzyja więc przejściu do stanu o mniejszej objętości, czyli do wody, co ułatwia topnienie w niższej temperaturze. To zjawisko jest kluczowe np. dla ruchu lodowców czy jazdy na łyżwach.
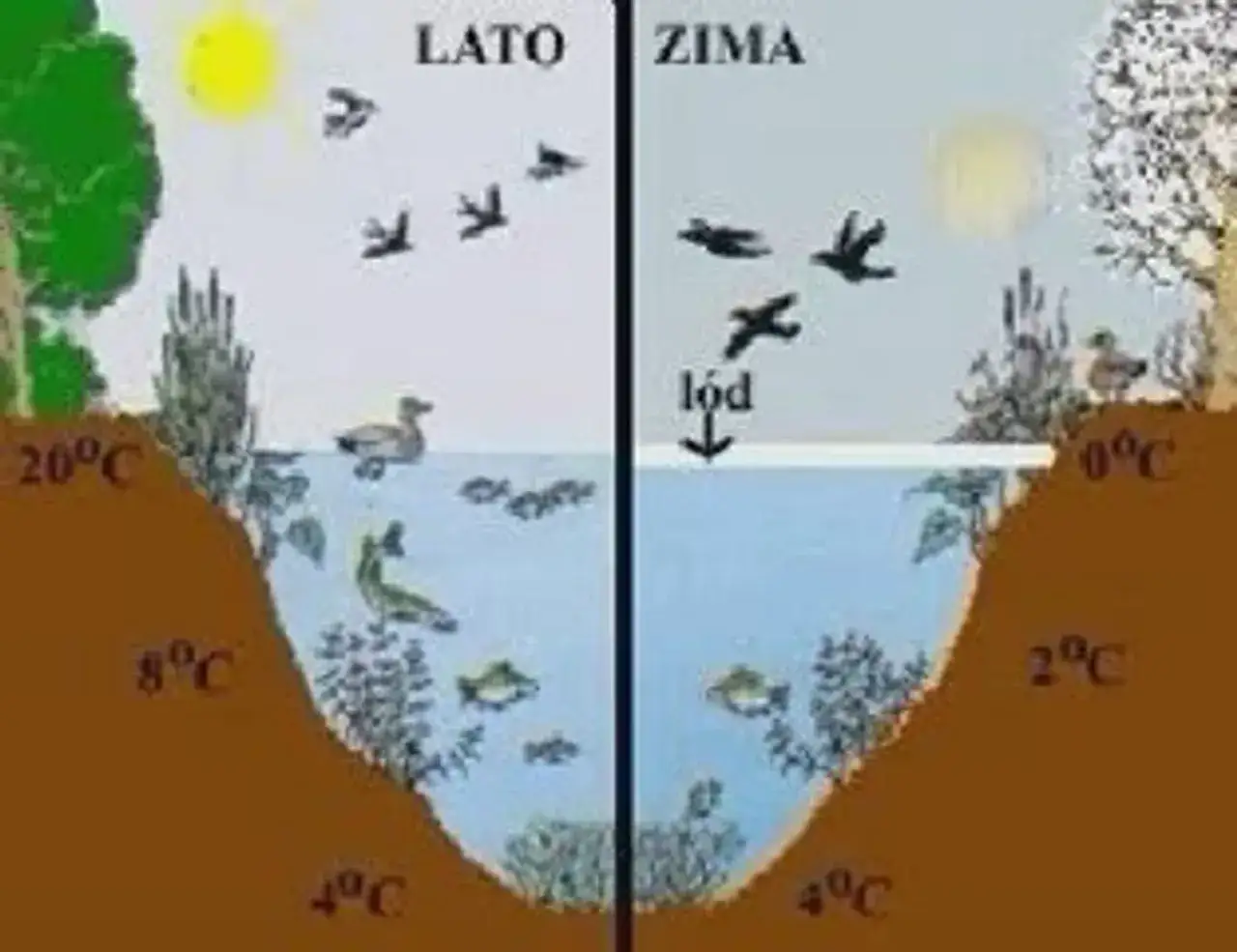
Anomalna rozszerzalność wody: Jak wykres tłumaczy, dlaczego lód pływa?
Anomalna rozszerzalność wody to kolejne fascynujące zjawisko, które ma ogromne konsekwencje dla życia na Ziemi. Woda, w przeciwieństwie do większości substancji, ma największą gęstość w temperaturze około 4°C. Oznacza to, że gdy ochładzamy ją od 4°C do 0°C, zamiast kurczyć się, zaczyna się rozszerzać. Podobnie, gdy ogrzewamy ją powyżej 4°C, również się rozszerza. To właśnie dlatego lód ma mniejszą gęstość niż woda i pływa po jej powierzchni. Ta właściwość jest absolutnie kluczowa dla życia w zbiornikach wodnych zimą. Dzięki niej lód tworzy izolacyjną warstwę na powierzchni, chroniąc głębsze warstwy wody przed zamarznięciem i pozwalając organizmom wodnym przetrwać zimę.Wykres a zjawiska specjalne: przechłodzenie i jego wpływ
Podczas gdy podstawowy wykres topnienia i krzepnięcia opisuje idealne warunki, w rzeczywistości możemy spotkać się z intrygującymi odstępstwami, takimi jak zjawisko przechłodzenia. To pokazuje, jak złożone mogą być procesy fizyczne.
Zjawisko przechłodzenia: Jak to możliwe, że woda ma ujemną temperaturę i nie zamarza?
Zjawisko przechłodzenia to prawdziwa fizyczna ciekawostka. Woda w bardzo czystym stanie, pozbawiona wszelkich zanieczyszczeń, pęcherzyków powietrza czy nierówności na ściankach naczynia (czyli tzw. ośrodków krystalizacji), może zostać schłodzona poniżej 0°C, a mimo to nie zamarznąć. Jest to stan metastabilny woda jest w stanie ciekłym, choć jej temperatura wskazuje, że powinna już być lodem. Wystarczy jednak niewielkie zaburzenie, na przykład delikatne potrząśnięcie naczyniem, wrzucenie drobinki kurzu, a nawet dotknięcie patyczkiem, by woda gwałtownie skrystalizowała, zamieniając się w lód.
Jak wyglądałby wykres dla przechłodzonej wody? Analiza przypadku
Jeśli na naszym wykresie uwzględnimy zjawisko przechłodzenia, zobaczymy intrygującą modyfikację. Odcinek oziębiania wody (ten skośny w dół) nie zatrzyma się na 0°C, ale będzie kontynuowany, a temperatura wody spadnie poniżej zera, na przykład do -5°C. W tym momencie, gdy nastąpi inicjacja krystalizacji (np. przez wspomniane wcześniej zaburzenie), temperatura gwałtownie wzrośnie z powrotem do 0°C. Dopiero wtedy rozpocznie się standardowy proces krzepnięcia, który będzie przebiegał w stałej temperaturze 0°C, aż cała woda zamarznie. To doskonały przykład tego, jak warunki początkowe i obecność zanieczyszczeń mogą wpływać na przebieg przemian fazowych.