Woda, substancja tak powszechna, że często nie doceniamy jej niezwykłych właściwości. Jedną z nich jest jej wyjątkowo wysokie ciepło właściwe, które odgrywa fundamentalną rolę w stabilizacji klimatu na Ziemi i umożliwia istnienie życia, jakie znamy. Zapraszam do zgłębienia tego fascynującego fenomenu, który chroni naszą planetę i nasze ciała przed gwałtownymi zmianami temperatury.
Wysokie ciepło właściwe wody klucz do stabilności klimatu i życia na Ziemi
- Ciepło właściwe wody to około 4200 J/(kg·K), co oznacza, że potrzeba znacznej energii, aby podnieść jej temperaturę. Jest to jedna z najwyższych wartości wśród powszechnych substancji.
- Główną przyczyną tej właściwości są wiązania wodorowe między polarnymi cząsteczkami wody, które muszą zostać zerwane, zanim energia zacznie zwiększać ruch cząsteczek, czyli podnosić temperaturę.
- Dzięki temu oceany i morza działają jako gigantyczne bufory termiczne, pochłaniając i oddając ciepło powoli, co łagodzi wahania temperatury na skalę globalną i regionalną.
- Wysokie ciepło właściwe wody w organizmach żywych (stanowiących do 85% masy komórek) zapewnia stabilną temperaturę wewnętrzną, chroniąc przed szokiem termicznym i wspierając homeostazę.
- Lód, o mniejszej gęstości niż woda, tworzy izolującą warstwę na powierzchni zbiorników, chroniąc głębsze warstwy przed zamarzaniem i umożliwiając przetrwanie organizmom wodnym zimą.
Zrozumieć fenomen: czym właściwie jest ciepło właściwe?
Zacznijmy od podstaw. Ciepło właściwe to nic innego jak ilość energii (ciepła) potrzebna do podniesienia temperatury 1 kilograma danej substancji o 1 stopień Celsjusza (lub 1 Kelwin). W przypadku wody wartość ta jest naprawdę imponująca i wynosi około 4200 dżuli na kilogram i kelwin (J/(kg·K)). Dla porównania, piasek ma ciepło właściwe około pięciokrotnie niższe! Ta wysoka wartość sprawia, że woda jest niezwykle efektywnym magazynem energii cieplnej, co ma kolosalne konsekwencje dla naszej planety.
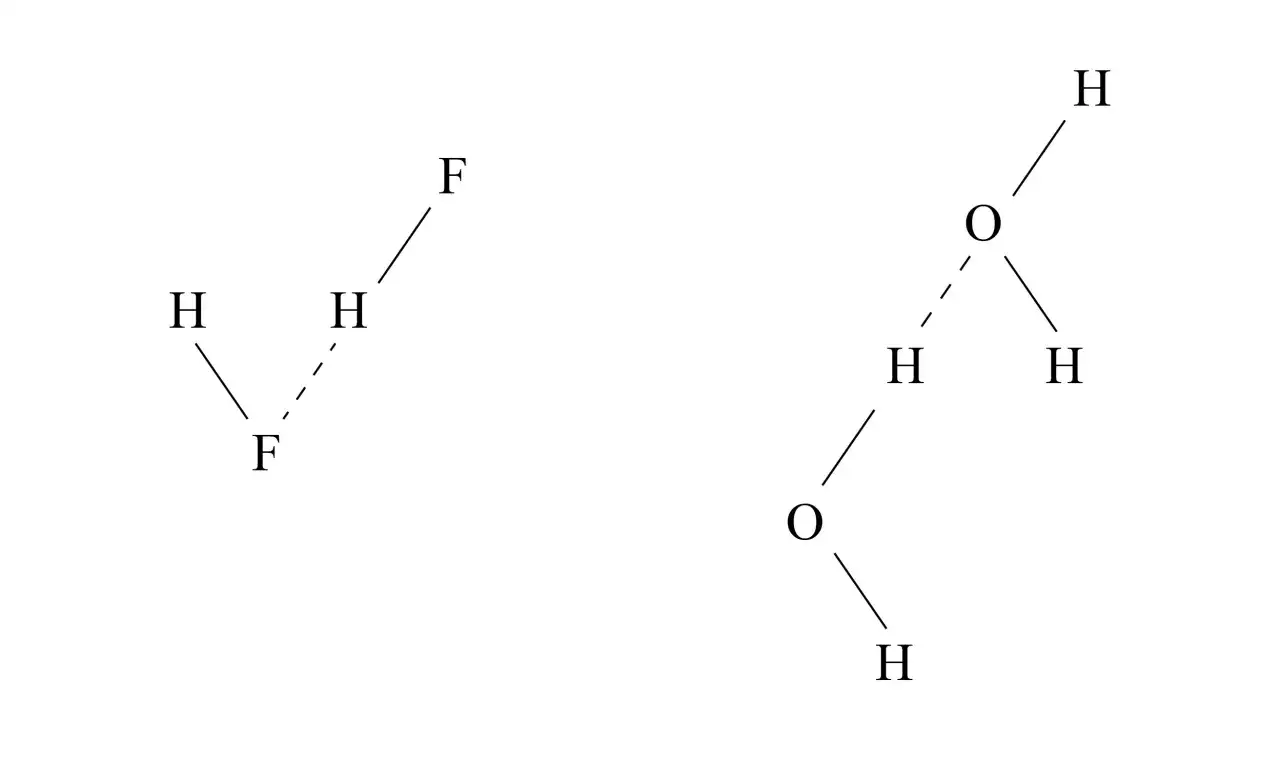
Sekret ukryty w strukturze cząsteczki H₂O: oto winowajca!
Klucz do zrozumienia wysokiego ciepła właściwego wody leży w jej budowie molekularnej. Cząsteczka wody (H₂O) jest polarna tlen przyciąga elektrony silniej niż wodór, tworząc częściowe ładunki ujemne na tlenie i dodatnie na wodorze. Te częściowe ładunki sprawiają, że cząsteczki wody silnie oddziałują ze sobą, tworząc tak zwane wiązania wodorowe. To właśnie te wiązania są głównym "winowajcą" i jednocześnie błogosławieństwem dla życia na Ziemi.
Jak wiązania wodorowe zmuszają wodę do "magazynowania" energii?
Wyobraźmy sobie, że dostarczamy energię do jakiejś cieczy. W większości substancji energia ta niemal od razu przekłada się na zwiększenie energii kinetycznej cząsteczek, co odczuwamy jako wzrost temperatury. W przypadku wody jest inaczej. Zanim temperatura wody zacznie rosnąć, znaczna część dostarczonej energii musi zostać zużyta na zerwanie licznych wiązań wodorowych, które utrzymują cząsteczki wody razem. Dopiero po ich osłabieniu lub zerwaniu, pozostała energia może zwiększyć ruch cząsteczek i podnieść temperaturę. To sprawia, że woda "opiera się" zmianom temperatury, działając jak bufor. Inne ciecze, pozbawione tak silnych wiązań międzycząsteczkowych, nagrzewają się znacznie szybciej, ponieważ dostarczona energia od razu zwiększa energię kinetyczną ich cząsteczek.
Praktyczne korzyści: jak ciepło właściwe wody wpływa na klimat i nasze życie
Jak oceany i morza regulują klimat na Ziemi?
Ogromne zbiorniki wodne, takie jak oceany i morza, są niczym gigantyczne bufory termiczne dla naszej planety. Dzięki wysokiemu ciepłu właściwemu, woda w nich pochłania olbrzymie ilości energii słonecznej w ciągu dnia i latem, nagrzewając się bardzo powoli. To zapobiega ekstremalnym upałom na lądzie. Zimą i w nocy, te same zbiorniki wodne powoli oddają zmagazynowane ciepło do atmosfery, łagodząc mrozy i zapobiegając gwałtownym spadkom temperatury. To właśnie dlatego klimat nadmorski jest znacznie bardziej stabilny i łagodny niż kontynentalny.
Gigantyczny bufor termiczny: dlaczego nad morzem jest chłodniej latem i cieplej zimą?
To zjawisko jest doskonale odczuwalne dla każdego, kto spędził wakacje nad morzem. Latem, gdy słońce mocno grzeje, temperatura powietrza nad lądem może osiągać wysokie wartości. Jednak nad morzem jest zazwyczaj przyjemniej. Dzieje się tak, ponieważ woda w morzu pochłania ogromne ilości energii, ale jej temperatura rośnie bardzo powoli. Powietrze nad chłodniejszą wodą również jest chłodniejsze. Zimą natomiast, gdy ląd szybko się wychładza, morze, które przez całe lato i jesień magazynowało ciepło, powoli je oddaje, ogrzewając okoliczne powietrze. To sprawia, że zimy nad morzem są znacznie łagodniejsze niż w głębi lądu, gdzie brak jest tego wodnego regulatora.Powolne parowanie i skraplanie jako globalny system transportu energii
Nie tylko samo magazynowanie ciepła przez wodę ma znaczenie. Procesy parowania i skraplania wody w atmosferze również odgrywają kluczową rolę w globalnym transporcie energii. Gdy woda paruje, pochłania energię (ciepło parowania), która jest następnie uwalniana, gdy para wodna skrapla się, tworząc chmury i opady. Ten ciągły cykl przenosi ogromne ilości energii z cieplejszych regionów Ziemi do chłodniejszych, dodatkowo stabilizując globalny klimat i rozprowadzając ciepło po całej planecie.
Dlaczego stabilność temperatury wody jest kluczowa dla życia?
Woda to nie tylko oceany i rzeki; to także główny składnik wszystkich organizmów żywych. Nasze komórki składają się w 75-85% z wody. Dzięki jej wysokiemu ciepłu właściwemu, wewnętrzna temperatura naszych ciał i wszystkich innych organizmów jest niezwykle stabilna i odporna na nagłe zmiany temperatury otoczenia. To kluczowe dla utrzymania homeostazy równowagi wewnętrznej organizmu i prawidłowego przebiegu niezliczonych procesów metabolicznych, które są wrażliwe na wahania temperatury.
Ochrona organizmów wodnych przed szokiem termicznym
Wyobraźmy sobie życie w jeziorze. Gdyby woda nagrzewała się i ochładzała tak szybko jak powietrze, organizmy wodne byłyby nieustannie narażone na drastyczne zmiany temperatury, co prowadziłoby do szoku termicznego i masowego wymierania. Na szczęście, dzięki wysokiemu ciepłu właściwemu, temperatura w zbiornikach wodnych zmienia się bardzo powoli. Ryby, rośliny wodne i inne stworzenia mają czas na adaptację do stopniowych zmian, co jest fundamentalne dla ich przetrwania.
Niezwykła anomalia: dlaczego lód unosi się na wodzie i tworzy warstwę ochronną?
To kolejna cudowna właściwość wody, ściśle związana z wiązaniami wodorowymi. W przeciwieństwie do większości substancji, lód ma mniejszą gęstość niż woda w stanie ciekłym. Oznacza to, że lód unosi się na powierzchni wody. Zimą, gdy temperatura spada poniżej zera, na powierzchni jezior i rzek tworzy się warstwa lodu. Ta warstwa działa jak naturalny izolator, chroniąc głębsze warstwy wody przed dalszym zamarzaniem. Dzięki temu życie pod lodem ryby, płazy, owady może przetrwać najsroższe mrozy, w stosunkowo stabilnych i cieplejszych warunkach.
Woda jako strażnik temperatury Twojego ciała
Jak woda w komórkach chroni Cię przed przegrzaniem i wychłodzeniem?
Woda w naszych komórkach działa jak osobisty termoregulator. Kiedy na zewnątrz jest gorąco, woda w ciele pochłania nadmiar ciepła, zapobiegając szybkiemu przegrzaniu. Kiedy jest zimno, powoli oddaje zmagazynowane ciepło, chroniąc nas przed gwałtownym wychłodzeniem. To właśnie dzięki tej właściwości nasza temperatura wewnętrzna utrzymuje się na stałym poziomie około 37°C, niezależnie od tego, czy spacerujemy po pustyni, czy po zaśnieżonym lesie.
Pot najskuteczniejszy naturalny klimatyzator i jego związek z ciepłem parowania
Oprócz wysokiego ciepła właściwego, woda ma także niezwykle wysokie ciepło parowania, co również jest bezpośrednio związane z wiązaniami wodorowymi. Aby woda zmieniła stan skupienia z ciekłego na gazowy (czyli wyparowała), potrzebuje ogromnej ilości energii. Nasz organizm wykorzystuje to zjawisko w procesie pocenia się. Kiedy pot paruje z powierzchni skóry, odbiera z niej bardzo duże ilości ciepła, skutecznie chłodząc ciało. To nasz naturalny i niezwykle efektywny system klimatyzacji, który pozwala nam funkcjonować nawet w bardzo wysokich temperaturach.
Wyobraź sobie świat bez tej supermocy wody
Jak wyglądałby dzień na plaży, gdyby woda nagrzewała się jak piasek?
Wyobraź sobie upalny dzień na plaży, ale z jednym kluczowym wyjątkiem: woda w morzu nagrzewa się tak szybko jak piasek. W ciągu dnia, zamiast orzeźwiającej kąpieli, weszlibyśmy do wrzącej niemal wody, która w ciągu kilku godzin osiągnęłaby temperaturę nie do zniesienia. Piasek, jak zwykle, byłby gorący. Ale prawdziwy szok nadszedłby w nocy. Piasek szybko by ostygł, ale woda również! Zamiast przyjemnie ciepłej wody, która oddaje ciepło do otoczenia, mielibyśmy do czynienia z lodowatą cieczą, która w ciągu kilku godzin straciła całe nagromadzone ciepło. Takie wahania byłyby katastrofalne.
Przeczytaj również: Masa czy ciężar? Zrozum różnicę raz na zawsze!
Czy życie mogłoby istnieć przy gwałtownych, dobowych skokach temperatury?
Gdyby woda miała niskie ciepło właściwe, dobowe wahania temperatury na Ziemi byłyby ekstremalne. W dzień temperatury mogłyby szybować do niewyobrażalnych wartości, a w nocy spadać poniżej zera w ciągu kilku godzin. Oceany i rzeki nagrzewałyby się i ochładzały błyskawicznie. W takich warunkach życie, jakie znamy, prawdopodobnie nie mogłoby istnieć. Organizmy nie byłyby w stanie utrzymać stabilnej temperatury wewnętrznej, a procesy biochemiczne ulegałyby denaturacji. Gwałtowne zmiany temperatury niszczyłyby komórki i tkanki. Można śmiało powiedzieć, że wysokie ciepło właściwe wody to jedna z fundamentalnych cech, która uczyniła Ziemię planetą zdolną do podtrzymywania życia.