Prosta instrukcja hodowli kryształów soli Twój domowy eksperyment naukowy
- Kluczem do sukcesu jest przygotowanie roztworu nasyconego w gorącej wodzie to podstawa, by kryształy w ogóle zaczęły rosnąć.
- Niezbędne materiały znajdziesz w większości domów: sól niejodowana, gorąca woda, słoik, nitka (najlepiej bawełniana lub wełniana) oraz patyczek.
- Pierwsze kryształki zobaczysz już po kilku dniach, ale na pełny wzrost, który naprawdę robi wrażenie, poczekaj cierpliwie od 1 do 3 tygodni.
- Dla najlepszych efektów, słoik postaw w spokojnym miejscu o stabilnej temperaturze, co zapewni wolne i równomierne parowanie wody.
- Najczęstsze problemy to zbyt mało soli w roztworze lub zbyt szybkie parowanie ale na wszystko są proste rozwiązania!
- Eksperyment jest bezpieczny, ale zawsze pamiętaj o nadzorze osoby dorosłej, szczególnie przy pracy z gorącą wodą.

Przygotuj swój zestaw małego naukowca
Zanim zagłębisz się w proces krystalizacji, musimy zebrać wszystkie potrzebne narzędzia. Dobra wiadomość jest taka, że większość z nich prawdopodobnie masz już w swojej kuchni lub szufladzie z przyborami.
Czego dokładnie potrzebujesz? Lista niezbędnych przedmiotów z Twojej kuchni
- Sól kuchenna (NaCl): Duża paczka! Pamiętaj, że sól niejodowana i bez antyzbrylaczy zazwyczaj daje lepsze, bardziej regularne kryształy, ale zwykła, jodowana sól też zadziała. Po prostu efekty mogą być nieco mniej spektakularne.
- Ciepła lub gorąca woda: Najlepiej prosto z czajnika, świeżo zagotowana.
- Przezroczysty słoik lub szklanka: Im większy, tym więcej miejsca na kryształy. Przezroczystość pozwoli Ci obserwować cały proces.
- Nitka lub sznurek: Bawełniana lub wełniana nitka sprawdzi się najlepiej. Ważne, aby była naturalna i nieco "włochata".
- Patyczek, ołówek lub kredka: Posłuży do zawieszenia nitki nad roztworem.
- Łyżka: Do mieszania.
- Opcjonalnie: spinacz biurowy: Jako obciążnik dla nitki, jeśli będzie potrzebny.
- Opcjonalnie: barwniki spożywcze: Jeśli chcesz nadać swoim kryształom niezwykłe kolory.
Sól soli nierówna: Czy rodzaj soli ma znaczenie dla wielkości kryształów?
Z mojego doświadczenia wynika, że choć do hodowli kryształów soli kuchennej (chlorku sodu, NaCl) nadaje się praktycznie każda sól, to jednak istnieją pewne niuanse. Jeśli marzą Ci się duże, piękne i regularne kryształy, postaw na sól niejodowaną i bez dodatku antyzbrylaczy. Te substancje mogą nieco zakłócać proces krystalizacji, prowadząc do tworzenia się mniejszych lub mniej idealnych form. Zwykła sól jodowana i tak zadziała, ale efekty mogą być po prostu mniej spektakularne.
Tajemnica idealnej nitki: Dlaczego bawełna i wełna sprawdzają się najlepiej?
Wybór odpowiedniej nitki to nie przypadek. Nitki z naturalnych materiałów, takich jak bawełna czy wełna, mają chropowatą, włochatą powierzchnię. To właśnie te drobne nierówności i włókienka stanowią idealne punkty zaczepienia dla pierwszych, mikroskopijnych kryształków soli. Działają jak "rusztowanie", na którym sól może się osadzać i stopniowo budować większe struktury. Gładkie, syntetyczne nitki nie oferują tylu punktów krystalizacji, co może spowolnić lub utrudnić proces.
Stwórz magiczny roztwór serce eksperymentu
Przygotowanie roztworu nasyconego to absolutny fundament naszego eksperymentu. Bez niego kryształy po prostu nie urosną. To właśnie w tym płynie tkwi cała magia, a właściwie chemia!
Klucz do sukcesu, czyli przepis na idealny roztwór nasycony
Roztwór nasycony to taki, w którym rozpuściła się maksymalna możliwa ilość substancji w naszym przypadku soli w danej temperaturze. Kiedy woda zacznie parować, sól nie będzie miała gdzie się podziać i zacznie osadzać się w postaci kryształów. Oto jak go przygotować:- Zagotuj wodę w czajniku. Pamiętaj o ostrożności gorąca woda to nie przelewki, zwłaszcza gdy eksperymentujesz z dziećmi.
- Wlej gorącą wodę do słoika, wypełniając go do około 3/4 wysokości.
- Zacznij dodawać sól, po jednej łyżeczce, i energicznie mieszaj, aż sól całkowicie się rozpuści.
- Kontynuuj dodawanie soli i mieszanie. W pewnym momencie zauważysz, że sól przestaje się rozpuszczać i zaczyna osadzać się na dnie słoika, nawet po intensywnym mieszaniu. To znak, że osiągnąłeś roztwór nasycony.
- Pozwól roztworowi ostygnąć przez około 15-20 minut. W tym czasie nadmiar soli może osiąść na dnie, co jest całkowicie normalne. Nie wlewaj do słoika nitki, gdy roztwór jest jeszcze bardzo gorący.
Gorąca woda Twój sprzymierzeniec: Dlaczego temperatura jest tak ważna?
Zastanawiałeś się, dlaczego upieram się przy gorącej wodzie? Odpowiedź jest prosta i tkwi w fizyce: ciepła woda jest w stanie rozpuścić znacznie więcej soli niż zimna. To kluczowe, ponieważ im więcej soli rozpuścisz na początku, tym bardziej "nasycony" będzie Twój roztwór. Gdy woda zacznie parować, stężenie soli będzie rosło, a jej nadmiar zacznie się krystalizować. Użycie gorącej wody to po prostu sprytny sposób na stworzenie idealnych warunków do szybkiego i efektywnego wzrostu kryształów.
Opcjonalny krok dla artystów: Jak zabarwić swoje kryształy na dowolny kolor?
Jeśli chcesz, aby Twoje kryształy miały nie tylko imponujący kształt, ale i piękny kolor, to mam dla Ciebie dobrą wiadomość! Wystarczy, że do świeżo przygotowanego, gorącego roztworu nasyconego dodasz kilka kropel barwnika spożywczego. Kolor roztworu przeniknie do tworzących się kryształów, nadając im fantastyczny odcień. Pamiętaj tylko, aby dodać barwnik przed zanurzeniem nitki, by kolor równomiernie się rozprowadził.
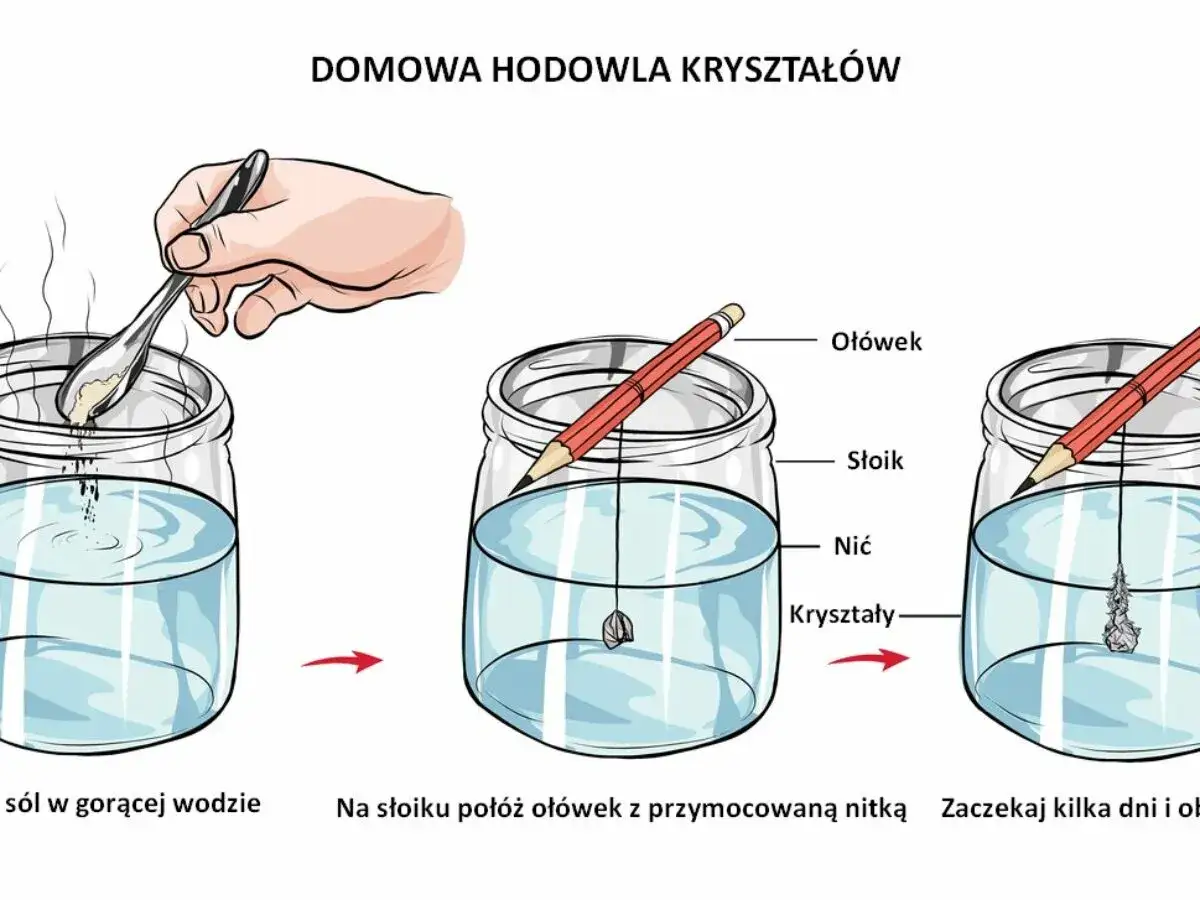
Rozpocznij hodowlę kryształów instrukcja krok po kroku
Mamy już przygotowany roztwór, teraz czas na najważniejszy moment uruchomienie naszej "fabryki" kryształów. To właśnie teraz zaczyna się prawdziwa zabawa!
Przygotowanie "rusztowania": Jak prawidłowo zamocować nitkę, by nie dotykała dna?
Prawidłowe zamocowanie nitki jest kluczowe, aby kryształy rosły tam, gdzie chcesz czyli na niej, a nie na dnie słoika. Oto jak to zrobić:
- Odetnij kawałek nitki o długości, która pozwoli jej swobodnie zwisać w słoiku, nie dotykając dna ani ścianek.
- Jeden koniec nitki przywiąż do środka patyczka, ołówka lub kredki.
- Jeśli nitka jest zbyt lekka i nie chce się zanurzyć, możesz na jej drugi koniec zawiązać mały spinacz biurowy posłuży jako obciążnik.
- Po ostygnięciu roztworu, połóż patyczek na wierzchu słoika tak, aby nitka z obciążnikiem (lub bez) zanurzyła się w roztworze. Upewnij się, że nitka wisi swobodnie i nie dotyka ani dna, ani ścianek słoika. To bardzo ważne, ponieważ kontakt z nimi może spowodować, że kryształy zaczną rosnąć w niepożądanych miejscach.
Wielkie zalewanie i cierpliwe oczekiwanie: Gdzie postawić słoik, aby kryształy rosły najpiękniejsze?
Teraz, gdy wszystko jest gotowe, postaw słoik w spokojnym miejscu, gdzie temperatura jest stabilna i nie ma przeciągów. Unikaj bezpośredniego światła słonecznego i miejsc blisko źródeł ciepła (np. kaloryferów). Dlaczego? Ponieważ wolniejsze parowanie wody sprzyja powstawaniu większych, bardziej regularnych i estetycznych kryształów. Szybkie parowanie często prowadzi do tworzenia się wielu małych, chaotycznych kryształków. Pierwsze, malutkie kryształki mogą pojawić się już po kilku dniach, ale na naprawdę okazałe formy trzeba poczekać od jednego do nawet trzech tygodni. Cierpliwość to cnota każdego naukowca!
Dziennik obserwacji: Jak dokumentować wzrost kryształów dzień po dniu?
Zachęcam Cię do prowadzenia prostego dziennika obserwacji. To fantastyczny sposób, by śledzić postępy i zrozumieć, jak działa proces krystalizacji. Codziennie, lub co drugi dzień, zanotuj datę, zrób szybki szkic lub zdjęcie, i opisz, co widzisz. Czy kryształy rosną? Czy zmieniły kształt? Czy pojawiły się nowe? To nie tylko świetna zabawa, ale także cenna lekcja naukowa, która uczy systematyczności i spostrzegawczości. Kto wie, może to początek kariery młodego chemika?
Coś poszło nie tak? Rozwiąż najczęstsze problemy
Nawet w najlepszych eksperymentach zdarzają się niespodzianki. Nie martw się, jeśli Twoje kryształy nie rosną dokładnie tak, jak sobie wyobrażałeś. Wiele problemów ma proste rozwiązania. Jako Igor Lis, pomogę Ci je zdiagnozować i naprawić.
Dlaczego moje kryształy nie chcą rosnąć? Sprawdź te 3 rzeczy!
Jeśli po kilku dniach na nitce nie widać żadnych kryształów, najprawdopodobniej problemem jest niewystarczająco nasycony roztwór. Innymi słowy, woda jest w stanie rozpuścić jeszcze więcej soli, więc nie ma "nadmiaru", który mógłby się krystalizować. Rozwiązanie: Wyjmij nitkę, ponownie podgrzej roztwór (np. w mikrofalówce lub w garnku), dodaj jeszcze więcej soli i mieszaj, aż przestanie się rozpuszczać. Poczekaj, aż ostygnie, i ponownie zanurz nitkę. Upewnij się też, że słoik stoi w miejscu, gdzie woda może swobodnie parować.
Ratunku, kryształy rosną wszędzie, tylko nie na nitce! Co robić?
To dość częsty problem. Jeśli kryształy osadzają się na dnie słoika lub na jego ściankach, zamiast na nitce, może to być spowodowane zbyt szybkim schłodzeniem roztworu po jego przygotowaniu lub obecnością zanieczyszczeń. Rozwiązanie: Przenieś słoik w miejsce o bardziej stabilnej, nieco chłodniejszej temperaturze, gdzie proces parowania będzie wolniejszy. Możesz też spróbować przelać roztwór do czystszego słoika, ostrożnie, aby nie wzburzyć osadu z dna, a następnie ponownie zanurzyć nitkę.
Zamiast kryształowego naszyjnika mam drobną "kaszę" jak to naprawić?
Kiedy zamiast dużych, lśniących kryształów pojawia się drobny, sypki osad, to niemal na pewno wina zbyt szybkiego parowania wody. Woda ucieka zbyt szybko, nie dając soli czasu na ułożenie się w duże, regularne struktury. Rozwiązanie: Przenieś naczynie w chłodniejsze, bardziej zacienione miejsce. Możesz również spróbować przykryć słoik luźno kawałkiem papieru lub folii spożywczej (niezbyt szczelnie, by powietrze mogło krążyć), co spowolni proces parowania. Cierpliwość jest kluczem do dużych kryształów!

Podnieś poziom trudności nowe wyzwania z krystalizacją
Gdy opanujesz już podstawy hodowli kryształów soli, świat nauki otwiera przed Tobą nowe możliwości. Nie ograniczaj się do jednego eksperymentu idź o krok dalej!
Sól kontra cukier: Zorganizuj zawody i porównaj efekty krystalizacji
Skoro udało Ci się z solą, dlaczego nie spróbować z inną popularną substancją? Przygotuj podobny eksperyment, ale tym razem użyj cukru. Zorganizuj "zawody" między solą a cukrem! Porównaj: * Kształty kryształów: Czy są takie same, czy zupełnie inne? * Rozmiary: Czy jedne rosną większe niż drugie? * Szybkość wzrostu: Które kryształy pojawiają się szybciej? * Teksturę: Jakie są w dotyku? To świetny sposób, by zrozumieć, że różne substancje krystalizują się w odmienny sposób, co jest fascynującą lekcją chemii.
Od kryształka do giganta: Jak wyhodować jeden, imponujący monokryształ?
Jeśli marzysz o wyhodowaniu jednego, naprawdę dużego i idealnego kryształu, musisz zastosować nieco inną strategię. To wyzwanie dla prawdziwych koneserów krystalizacji! Aby wyhodować imponujący monokryształ, najpierw wyhoduj kilka małych kryształków soli. Następnie wybierz jeden, idealny, mały kryształek to będzie Twój "zarodek". Przywiąż go do nitki i przenieś do świeżego, nasyconego roztworu soli. Kluczem jest teraz bardzo powolne parowanie wody. Możesz to osiągnąć, stawiając słoik w chłodniejszym miejscu lub częściowo przykrywając go. Cały proces zajmie znacznie więcej czasu, ale efekt będzie tego wart jeden, lśniący, ogromny kryształ!
Co dalej z gotowymi kryształami? Kreatywne pomysły na ich wykorzystanie
- Dekoracje: Gotowe kryształy mogą stać się piękną, oryginalną dekoracją w Twoim domu. Umieść je w małych słoiczkach, na podstawkach, a nawet stwórz z nich "drzewko" kryształowe.
- Elementy biżuterii: Mniejsze, ładne kryształki można delikatnie przykleić do baz biżuteryjnych, tworząc unikatowe kolczyki, wisiorki czy bransoletki.
- Prezenty: Ręcznie wyhodowane kryształy to fantastyczny, personalizowany prezent dla bliskich, zwłaszcza dla miłośników nauki i niezwykłych przedmiotów.
- Pomoce edukacyjne: Mogą służyć jako namacalny przykład krystalizacji podczas lekcji chemii lub fizyki w domu czy w szkole.
Magia czy nauka? Zrozum, dlaczego kryształy rosną
Na pierwszy rzut oka, rosnące kryształy mogą wydawać się magią. Ale za tym pięknym zjawiskiem stoi czysta nauka chemia i fizyka w akcji. Zrozumienie tego procesu sprawi, że eksperyment będzie jeszcze bardziej fascynujący.
Czym jest krystalizacja i dlaczego woda paruje, a sól zostaje?
Proces, który obserwujemy, to krystalizacja. Kiedy przygotowujemy roztwór nasycony, woda jest wypełniona cząsteczkami soli, które są w niej rozpuszczone. Z czasem, woda zaczyna parować, czyli przechodzić ze stanu ciekłego w gazowy i ulatniać się do atmosfery. Cząsteczki soli jednak nie parują pozostają w słoiku. W miarę jak wody ubywa, stężenie soli w pozostałym roztworze wzrasta. W końcu staje się tak wysokie, że roztwór jest "przesycony" nie jest już w stanie utrzymać tak dużej ilości soli w stanie rozpuszczonym. W tym momencie cząsteczki soli zaczynają się wytrącać z roztworu i, co najważniejsze, układają się w regularne, powtarzalne struktury geometryczne czyli właśnie w kryształy. Nitka działa jak idealne miejsce, gdzie ten proces może się rozpocząć i kontynuować.
Przeczytaj również: Bezpieczna elektroliza wody w domu? Zrób to z sodą oczyszczoną!
Czego uczy nas ten eksperyment? Podsumowanie Twojej przygody z chemią
Ten prosty eksperyment to znacznie więcej niż tylko zabawa. To praktyczna lekcja chemii, która w przystępny sposób wprowadza nas w świat nauki. Uczy nas o takich pojęciach jak rozpuszczalność (ile substancji może rozpuścić się w cieczy), nasycenie (moment, gdy ciecz nie może już rozpuścić więcej substancji), parowanie (proces przechodzenia wody w gaz) oraz oczywiście o tworzeniu się kryształów i ich regularnych strukturach. Przede wszystkim jednak, pokazuje, że nauka może być fascynująca, dostępna dla każdego i pełna niespodzianek. Mam nadzieję, że Twoja przygoda z krystalizacją zainspirowała Cię do dalszych odkryć!

