W dzisiejszych czasach, kiedy dążymy do świadomego i bezpiecznego dbania o zdrowie, zrozumienie podstawowych różnic między powszechnie stosowanymi substancjami jest kluczowe. Ten artykuł ma na celu rozłożenie na czynniki pierwsze chemicznych i praktycznych różnic między wodą utlenioną a spirytusem, aby każdy mógł używać ich świadomie i skutecznie w codziennym życiu.
Woda utleniona a spirytus: Fundamentalne różnice chemiczne i ich wpływ na działanie
- Woda utleniona (H₂O₂) to nieorganiczny nadtlenek, a spirytus (C₂H₅OH) to organiczny alkohol.
- H₂O₂ działa utleniająco poprzez nietrwałe wiązanie tlen-tlen, uwalniając tlen, co mechanicznie oczyszcza rany.
- C₂H₅OH denaturuje białka drobnoustrojów dzięki grupie hydroksylowej, wykazując największą skuteczność w stężeniu około 70% do dezynfekcji skóry.
- Woda utleniona jest niestabilna i łatwo się rozkłada, natomiast spirytus jest lotny i łatwopalny.
- Obie substancje nie są zalecane do rutynowego stosowania na otwarte rany ze względu na potencjalne uszkodzenie zdrowych tkanek i spowalnianie gojenia.
Dwa filary domowej apteczki skąd biorą się fundamentalne różnice?
Zarówno woda utleniona, jak i spirytus to substancje, które od lat goszczą w naszych domowych apteczkach. Często sięgamy po nie intuicyjnie, traktując jako uniwersalne środki do odkażania. Jednakże, pomimo że oba są bezbarwnymi płynami, ich chemiczna natura jest zupełnie inna. To właśnie te fundamentalne różnice w budowie cząsteczkowej determinują ich odmienne właściwości, mechanizmy działania i, co najważniejsze, zastosowania. Zrozumienie tego pozwala na ich bezpieczne i efektywne wykorzystanie.
Wzór chemiczny jako kod DNA substancji: Poznaj H₂O₂ i C₂H₅OH
Kluczem do zrozumienia różnic między tymi substancjami jest ich wzór chemiczny. Woda utleniona to naukowo nadtlenek wodoru, o wzorze H₂O₂. Jest to związek nieorganiczny, należący do grupy nadtlenków. Z kolei spirytus, czyli etanol, ma wzór C₂H₅OH i jest związkiem organicznym z grupy alkoholi. Te podstawowe różnice w klasyfikacji chemicznej są kluczowe i z nich wynikają wszystkie dalsze odmienności w ich właściwościach i zastosowaniach.
Co decyduje o ich właściwościach? Porównanie budowy cząsteczek
Woda utleniona: Moc niestabilnego wiązania tlen-tlen (-O-O-)
Cząsteczka wody utlenionej (H₂O₂) jest niezwykle interesująca. Składa się z dwóch atomów wodoru i dwóch atomów tlenu, ale to, co ją wyróżnia, to obecność nietrwałego wiązania tlen-tlen (-O-O-). To właśnie to wiązanie jest jej piętą achillesową i jednocześnie źródłem jej mocy. Cząsteczka H₂O₂ ma niepłaską strukturę, co dodatkowo wpływa na jej reaktywność. Niestabilność wiązania nadtlenkowego sprawia, że woda utleniona jest silnym utleniaczem i łatwo ulega rozkładowi, uwalniając tlen atomowy, co jest podstawą jej działania.
Spirytus (etanol): Rola grupy hydroksylowej (-OH) w świecie organicznym
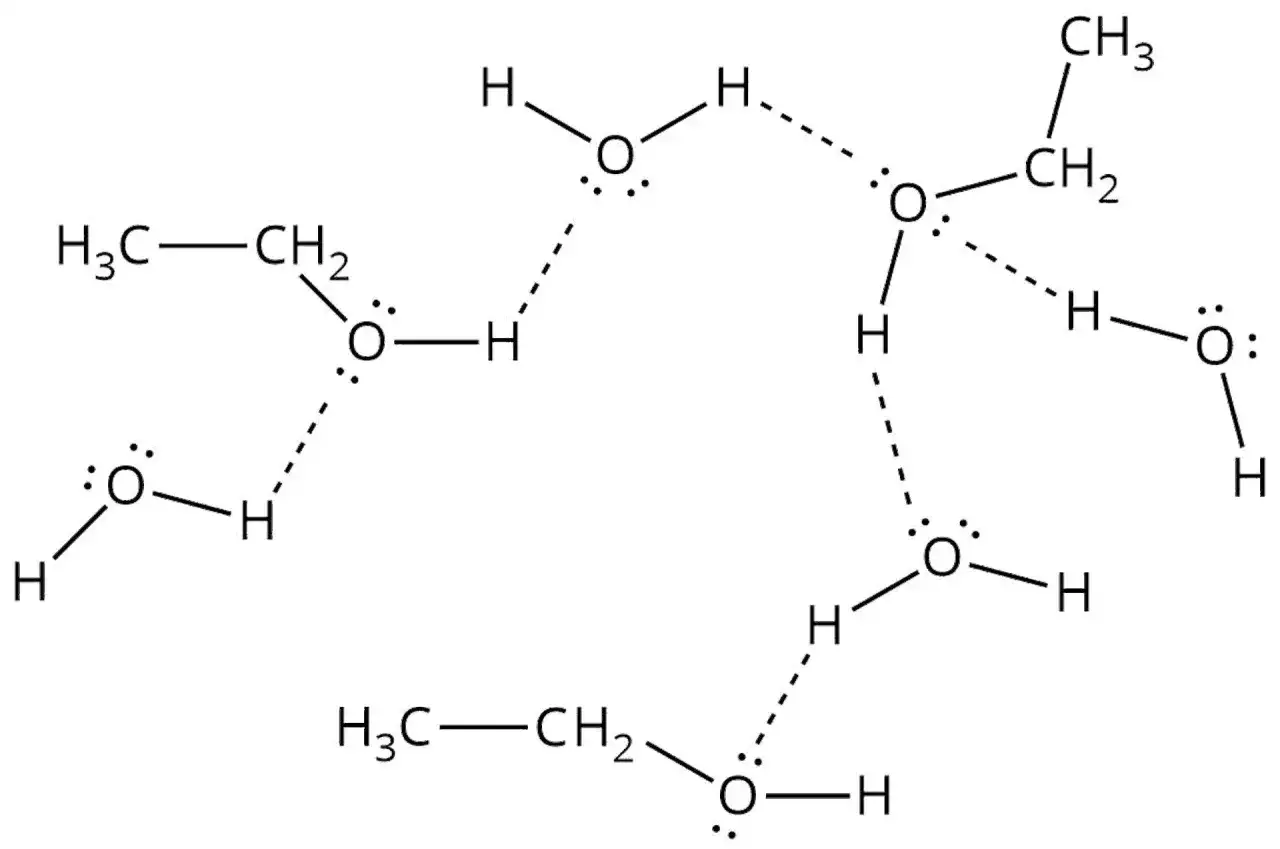
Etanol (C₂H₅OH) to typowy alkohol. Jego budowa opiera się na dwuwęglowym łańcuchu alkilowym (grupa etylowa, -C₂H₅), do którego przyłączona jest grupa hydroksylowa (-OH). To właśnie ta grupa funkcjonalna definiuje etanol jako alkohol i nadaje mu charakterystyczne właściwości. Grupa -OH sprawia, że etanol jest polarny, dobrze rozpuszczalny w wodzie i zdolny do tworzenia wiązań wodorowych. Co ważne w kontekście dezynfekcji, to właśnie obecność grupy hydroksylowej umożliwia mu denaturację białek, co jest kluczowe dla jego działania biobójczego.
Wizualne zestawienie: Jak struktura wpływa na zachowanie obu płynów?
| Cecha strukturalna | Woda utleniona (H₂O₂) | Spirytus (C₂H₅OH) |
|---|---|---|
| Typ związku | Nieorganiczny nadtlenek | Organiczny alkohol |
| Charakterystyczne wiązania/grupy | Nietrwałe wiązanie tlen-tlen (-O-O-) | Grupa hydroksylowa (-OH) |
| Podstawowa reaktywność | Silny utleniacz | Rozpuszczalnik organiczny, denaturator białek |
| Stabilność | Niestabilna, łatwo się rozkłada | Stabilna chemicznie, ale lotna |
Jak działają w praktyce? Mechanizmy dezynfekcji
Wybuchowa reakcja wody utlenionej: Jak piana i tlen oczyszczają ranę?
Mechanizm działania antyseptycznego wody utlenionej jest dość widowiskowy. Kiedy H₂O₂ styka się z tkankami, krwią lub ropą, wchodzi w reakcję z enzymem zwanym katalazą. Katalaza, obecna w większości komórek, gwałtownie rozkłada nadtlenek wodoru na wodę i tlen atomowy. To właśnie ten szybko uwalniający się tlen powoduje charakterystyczne pienienie się. Piana ta mechanicznie wypłukuje zanieczyszczenia, martwe tkanki i drobnoustroje z rany. Dodatkowo, tlen atomowy jest silnym utleniaczem, który uszkadza składniki komórkowe bakterii, wirusów i grzybów, co prowadzi do ich zniszczenia.
Cichy zabójca drobnoustrojów: Na czym polega denaturacja białek przez spirytus?
Spirytus działa inaczej, ale równie skutecznie. Jego biobójcze właściwości wynikają głównie z denaturacji białek. Etanol wnika do komórek mikroorganizmów i powoduje nieodwracalne zmiany w strukturze ich białek zarówno tych budulcowych, jak i enzymatycznych, które są niezbędne do życia i funkcjonowania komórki. Ponadto, spirytus uszkadza błony lipidowe bakterii oraz osłonki lipidowe niektórych wirusów, co prowadzi do ich dezaktywacji. To "rozpuszczenie" i zniszczenie kluczowych struktur komórkowych sprawia, że mikroorganizmy tracą zdolność do przetrwania i rozmnażania się.
Dlaczego stężenie ma znaczenie? Tajemnica 70% roztworu spirytusu

To może wydawać się sprzeczne z intuicją, ale spirytus wykazuje największą skuteczność antyseptyczną w stężeniu około 70%, a nie w czystej postaci (np. 96%). Dlaczego? Otóż woda odgrywa tu kluczową rolę. Jest ona niezbędna do procesu denaturacji białek bez wody białka nie koagulują tak efektywnie. Woda ułatwia również penetrację alkoholu do wnętrza komórek mikroorganizmów. Gdy używamy spirytusu o zbyt wysokim stężeniu (np. 96%), alkohol powoduje błyskawiczną koagulację białek na powierzchni komórki bakteryjnej, tworząc swoistą "skorupę". Ta skorupa działa jak bariera ochronna, uniemożliwiając alkoholowi wniknięcie głębiej i zniszczenie całej komórki. Roztwór 70% pozwala na bardziej stopniową i skuteczną denaturację białek w całym mikroorganizmie.
Właściwości fizykochemiczne: co odróżnia je w codziennym użyciu?
Palność i lotność: Dlaczego spirytus jest zagrożeniem pożarowym, a woda utleniona nie?
Jedną z najbardziej oczywistych różnic w codziennym użyciu jest palność i lotność. Spirytus (etanol) to ciecz bardzo lotna, co oznacza, że łatwo paruje, a jego opary są łatwopalne. Właśnie dlatego spirytus stanowi zagrożenie pożarowe i należy go przechowywać z dala od źródeł ognia. Czysty etanol wrze już w temperaturze 78,3°C. Woda utleniona, w stężeniach domowych (3%), to głównie woda, a sam nadtlenek wodoru w tych stężeniach nie wykazuje właściwości łatwopalnych. To sprawia, że jest bezpieczniejsza w przechowywaniu pod kątem ryzyka pożaru.
Stabilność i trwałość: Która substancja szybciej traci swoje właściwości i dlaczego?
Jeśli chodzi o stabilność, woda utleniona jest substancją znacznie bardziej nietrwałą. Jak już wspomniałem, wiązanie -O-O- jest słabe i łatwo ulega rozerwaniu. Pod wpływem światła, ciepła, a nawet zanieczyszczeń metalicznych czy enzymów, woda utleniona rozkłada się na wodę i tlen. Dlatego jest sprzedawana w ciemnych butelkach i ma ograniczony termin ważności po otwarciu. Spirytus natomiast jest chemicznie stabilniejszy. Nie rozkłada się w ten sposób, ale jest bardzo lotny, co oznacza, że z otwartego pojemnika szybko wyparuje, tracąc swoje stężenie i tym samym skuteczność.
Reaktywność: Utleniacz kontra związek organiczny
Podsumowując, różnice w reaktywności są fundamentalne. Woda utleniona jest silnym utleniaczem. Jej działanie polega na oddawaniu tlenu, który reaguje z innymi substancjami, niszcząc je. To sprawia, że jest skuteczna w usuwaniu plam, wybielaniu czy niszczeniu drobnoustrojów. Spirytus natomiast działa jako rozpuszczalnik organiczny i środek denaturujący. Nie oddaje tlenu, ale wchodzi w interakcje z białkami i lipidami, zmieniając ich strukturę. To właśnie ta różnica w mechanizmie chemicznym sprawia, że mają tak odmienne zastosowania i profile bezpieczeństwa.
Medyczne zastosowanie: kiedy i dlaczego wybrać właściwy środek?
Otwarta rana: Dlaczego współczesna medycyna odradza stosowanie obu tych substancji?
Wbrew powszechnym przekonaniom i długoletniej praktyce, współczesne zalecenia medyczne, w tym te wydawane przez Polskie Towarzystwo Leczenia Ran, odradzają rutynowe stosowanie zarówno wody utlenionej, jak i spirytusu na otwarte, głębokie rany. Dlaczego?
"Polskie Towarzystwo Leczenia Ran nie zaleca rutynowego stosowania wody utlenionej do odkażania ran, ponieważ może ona uszkadzać zdrowe komórki (fibroblasty) i spowalniać proces gojenia oraz tworzenia się ziarniny."
Moje doświadczenie jako Igor Lis potwierdza, że choć piana z wody utlenionej może mechanicznie oczyścić ranę, to jej silne właściwości utleniające nie rozróżniają między bakteriami a zdrowymi komórkami skóry, co może opóźniać proces regeneracji. Spirytus z kolei, choć skuteczny w dezynfekcji, powoduje silny ból i pieczenie na otwartej ranie, a także uszkadza delikatne tkanki, co również nie sprzyja szybkiemu gojeniu.
Dezynfekcja skóry: Kiedy spirytus jest lepszym wyborem?
Mimo powyższych zastrzeżeń, spirytus ma swoje niezastąpione miejsce w medycynie i higienie. Jest on preferowanym środkiem do dezynfekcji nieuszkodzonej skóry, na przykład przed zastrzykami, pobraniem krwi czy drobnymi zabiegami chirurgicznymi. Jego szybkie działanie biobójcze i odparowywanie sprawiają, że jest wygodny i efektywny. Ponadto, spirytus jest kluczowym składnikiem wielu żeli i płynów do dezynfekcji rąk. W formie spirytusu salicylowego (roztwór kwasu salicylowego w etanolu) znajduje zastosowanie w odkażaniu otarć, pielęgnacji cery trądzikowej czy w leczeniu niektórych zmian skórnych.
Przeczytaj również: Niewidzialny atrament z cytryny: Utlenianie poznaj jego sekret
Ryzyko i skutki uboczne: Jak ich budowa chemiczna przekłada się na podrażnienia i uszkodzenia tkanek?
Budowa chemiczna i mechanizmy działania obu substancji bezpośrednio przekładają się na ich potencjalne ryzyka i skutki uboczne. Silne właściwości utleniające H₂O₂, choć skuteczne przeciwko drobnoustrojom, mogą również uszkadzać zdrowe komórki skóry, prowadząc do podrażnień, a nawet spowalniając gojenie. Z kolei zdolność C₂H₅OH do denaturacji białek i odwadniania sprawia, że nałożony na otwartą ranę powoduje silny ból, pieczenie i może wysuszać skórę. Długotrwałe stosowanie spirytusu na skórę, nawet nieuszkodzoną, może prowadzić do jej przesuszenia, podrażnień i uszkodzenia naturalnej bariery ochronnej. Dlatego tak ważne jest, aby zawsze stosować te substancje zgodnie z przeznaczeniem i zaleceniami, pamiętając o ich chemicznych właściwościach.
Chemia bez tajemnic: kluczowe różnice, które warto zapamiętać
| Cecha | Woda utleniona (H₂O₂) | Spirytus (C₂H₅OH) |
|---|---|---|
| Typ związku chemicznego | Nieorganiczny nadtlenek | Organiczny alkohol |
| Charakterystyczna grupa/wiązanie | Nietrwałe wiązanie -O-O- | Grupa hydroksylowa -OH |
| Mechanizm działania | Uwalnianie tlenu atomowego, utlenianie, mechaniczne oczyszczanie | Denaturacja białek, uszkodzenie błon lipidowych |
| Kluczowe właściwości fizykochemiczne | Silny utleniacz, niestabilna, niepalna (w stęż. domowym) | Rozpuszczalnik, lotny, łatwopalny, największa skuteczność w 70% |
| Zalecenia medyczne (otwarte rany) | Nie zalecany (uszkadza zdrowe tkanki, spowalnia gojenie) | Nie zalecany (ból, pieczenie, uszkadza tkanki) |
| Zalecenia medyczne (dezynfekcja skóry) | Głównie do wstępnego oczyszczania zanieczyszczonych ran | Skuteczny do dezynfekcji nieuszkodzonej skóry (np. przed zastrzykiem) |

