Zrozumienie, jak szczepionki działają na poziomie komórkowym, jest kluczowe dla docenienia ich roli w ochronie zdrowia. W tym artykule, jako Igor Lis, pragnę szczegółowo wyjaśnić fascynujące mechanizmy, dzięki którym szczepionki uczą nasz układ odpornościowy tworzenia długotrwałej pamięci immunologicznej, przygotowując go na przyszłe spotkania z patogenami.
Szczepionki uczą układ odpornościowy, jak budować długotrwałą pamięć immunologiczną
- Szczepionki wprowadzają antygeny, które stymulują odporność bez wywoływania choroby, prowadząc do powstania pamięci immunologicznej.
- Komórki prezentujące antygen (APC), takie jak komórki dendrytyczne, pochłaniają i prezentują fragmenty antygenów limfocytom.
- Aktywacja limfocytów T (pomocniczych i cytotoksycznych) koordynuje odpowiedź i niszczy zainfekowane komórki.
- Aktywowane limfocyty B przekształcają się w komórki plazmatyczne, produkując przeciwciała neutralizujące patogeny.
- Kluczowe jest powstawanie długożyjących komórek pamięci T i B, które zapewniają szybką i silną odpowiedź przy ponownym kontakcie z patogenem.
- Nowoczesne szczepionki mRNA instruują komórki do produkcji antygenów, skutecznie stymulując obie gałęzie odporności.
Podstawowym celem każdej szczepionki jest "wytrenowanie" naszego układu odpornościowego. Wprowadzamy do organizmu antygeny mogą to być osłabione lub inaktywowane patogeny, ich fragmenty, a nawet "instrukcje" do ich produkcji, jak w przypadku szczepionek mRNA. Co ważne, te antygeny nie wywołują choroby, lecz stymulują odpowiedź immunologiczną. Cały ten proces ma na celu wytworzenie pamięci immunologicznej, która jest fundamentem długotrwałej ochrony. Dzięki niej, przy ponownym kontakcie z rzeczywistym patogenem, nasz organizm może zareagować znacznie szybciej i skuteczniej, często zanim zdążą pojawić się objawy choroby.
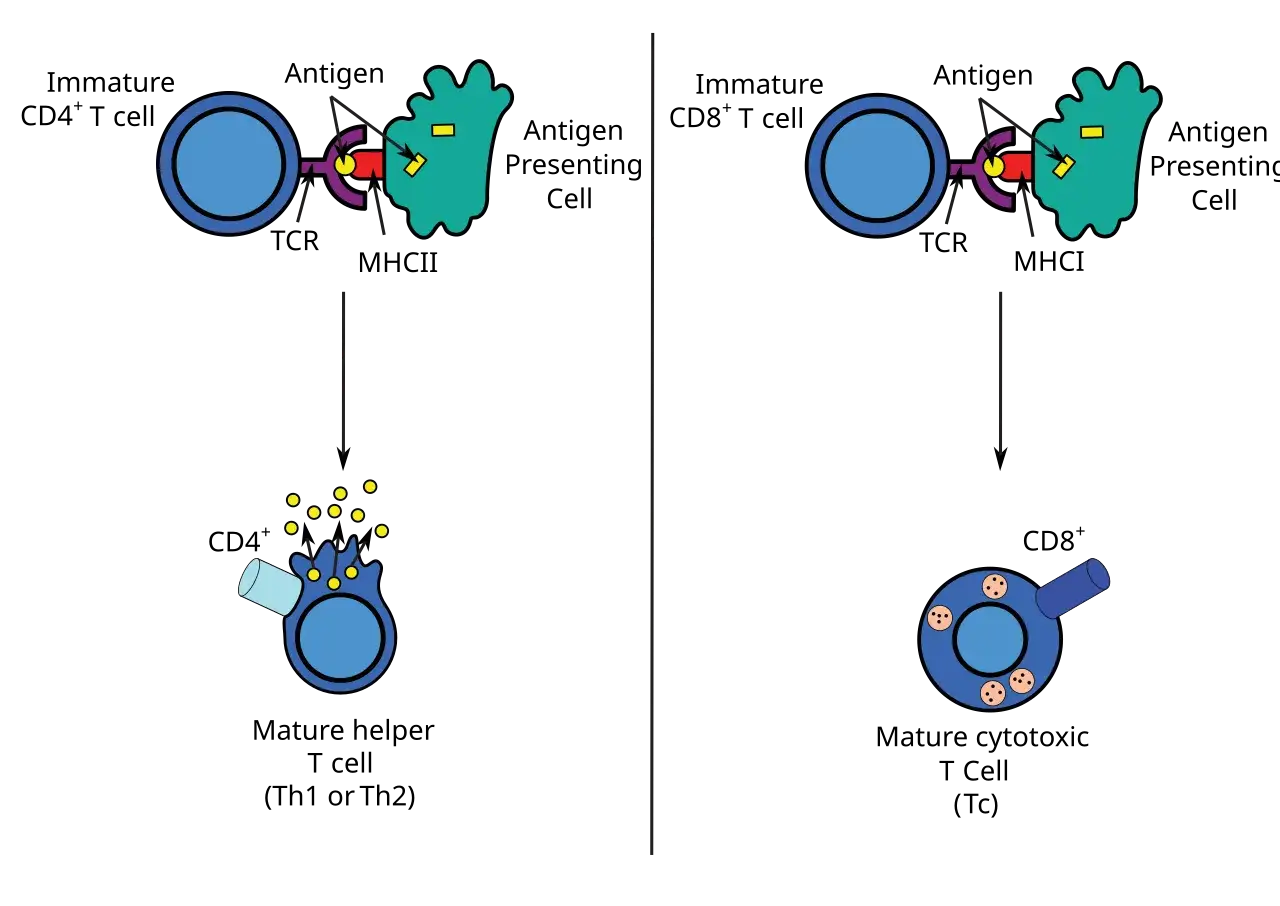
Prezentacja antygenu: jak komórki rozpoznają sygnał ze szczepionki
Kiedy szczepionka zostanie podana, jej antygeny nie pozostają obojętne. Są one natychmiast pochłaniane i przetwarzane przez wyspecjalizowane komórki naszego układu odpornościowego, zwane komórkami prezentującymi antygen (APC). Do najważniejszych z nich należą komórki dendrytyczne i makrofagi. Ich zadaniem jest "rozłożenie" antygenu na mniejsze fragmenty i zaprezentowanie ich na swojej powierzchni za pomocą specjalnych cząsteczek, zwanych głównym układem zgodności tkankowej (MHC). Po tym etapie, APC migrują do węzłów chłonnych strategicznych punktów, gdzie dochodzi do aktywacji kolejnych, kluczowych komórek odpornościowych.Rola komórek dendrytycznych: pierwsi strażnicy Twojej odporności
Wśród APC, komórki dendrytyczne zasługują na szczególną uwagę. Są to prawdziwi "strażnicy" naszej odporności, niezwykle efektywni w wychwytywaniu antygenów i prezentowaniu ich. Ich unikalna zdolność do migracji z miejsca infekcji (lub podania szczepionki) do węzłów chłonnych sprawia, że są idealnymi "posłańcami", którzy informują resztę układu odpornościowego o potencjalnym zagrożeniu. To właśnie dzięki nim sygnał ze szczepionki może zostać przetworzony i przekazany dalej z maksymalną efektywnością.
Od antygenu do informacji: jak fragment patogenu staje się sygnałem do działania?
Proces przetwarzania i prezentacji antygenu jest niezwykle precyzyjny. Gdy APC pochłonie antygen, enzymy wewnątrz komórki rozkładają go na małe peptydy. Te peptydy są następnie "ładowane" na cząsteczki MHC i wystawiane na zewnątrz komórki. To właśnie ta prezentacja fragmentu antygenu na cząsteczce MHC jest kluczowym "sygnałem do działania" dla układu odpornościowego. To tak, jakby APC pokazywała innym komórkom odpornościowym "zdjęcie poszukiwanego", informując je, czego mają szukać i zwalczać.
Aktywacja limfocytów T: koordynatorzy i zabójcy infekcji
W węzłach chłonnych, gdzie APC już dotarły z przetworzonymi antygenami, dochodzi do kluczowego spotkania. APC aktywują tam limfocyty T pomocnicze (CD4+). Rozpoznanie antygenu przez limfocyt T prowadzi do jego namnażania i różnicowania. Limfocyty T pomocnicze odgrywają rolę prawdziwych koordynatorów całej odpowiedzi immunologicznej, produkując cytokiny molekuły sygnałowe, które "dyrygują" innymi komórkami odpornościowymi, w tym aktywując limfocyty B. Co więcej, niektóre szczepionki, zwłaszcza te "żywe", mRNA i wektorowe, stymulują również limfocyty T cytotoksyczne (CD8+). Te komórki są prawdziwymi "zabójcami", zdolnymi do niszczenia komórek zainfekowanych przez patogeny, co jest niezwykle ważne w walce z wirusami.
Limfocyty T pomocnicze (CD4+): koordynatorzy odpowiedzi immunologicznej
Limfocyty T CD4+ są niczym dowódcy w armii odpornościowej. Po aktywacji zaczynają produkować różnorodne cytokiny, które pełnią funkcje informacyjne i regulacyjne. Niektóre cytokiny stymulują namnażanie innych limfocytów T, inne wspomagają aktywację limfocytów B i produkcję przeciwciał, a jeszcze inne rekrutują makrofagi do walki. Ich centralna rola w orkiestrowaniu zarówno odporności humoralnej (przeciwciała), jak i komórkowej (komórki T) sprawia, że są absolutnie niezbędne dla skutecznej odpowiedzi poszczepiennej.
Limfocyty T cytotoksyczne (CD8+): cisi zabójcy zainfekowanych komórek
Limfocyty T CD8+, często nazywane "komórkami T zabójcami", są wyspecjalizowane w rozpoznawaniu i eliminowaniu komórek gospodarza, które zostały zainfekowane przez wirusy lub inne patogeny wewnątrzkomórkowe. Dzieje się to poprzez rozpoznawanie fragmentów patogenów prezentowanych na cząsteczkach MHC klasy I na powierzchni zainfekowanych komórek. Po rozpoznaniu, limfocyty CD8+ uwalniają substancje, które indukują apoptozę (programowaną śmierć komórki) w zainfekowanej komórce, zapobiegając dalszemu rozprzestrzenianiu się patogenu. Ich obecność i aktywacja są kluczowe dla pełnej ochrony, zwłaszcza przed wirusami.
Limfocyty B i produkcja przeciwciał: uruchamianie fabryki obronnej
Równolegle do aktywacji limfocytów T, w węzłach chłonnych dochodzi do aktywacji limfocytów B. Często potrzebują one "pomocy" ze strony aktywowanych limfocytów T pomocniczych, aby w pełni się rozwinąć. Gdy limfocyt B rozpozna antygen i otrzyma sygnały od limfocytu T pomocniczego, rozpoczyna się jego intensywne namnażanie (ekspansja klonalna) i różnicowanie w komórki plazmatyczne. Te komórki są prawdziwymi "fabrykami" przeciwciał, masowo produkującymi te białka, które krążą we krwi i mogą neutralizować patogeny, blokując im możliwość infekowania komórek.
Od rozpoznania do działania: jak limfocyt B staje się komórką plazmatyczną?
Proces transformacji limfocytu B w komórkę plazmatyczną jest fascynujący. Początkowo, limfocyt B rozpoznaje antygen za pomocą swoich receptorów powierzchniowych. Następnie, przy wsparciu limfocytów T pomocniczych, ulega aktywacji. Aktywacja ta prowadzi do szybkiego podziału komórkowego klonalnej ekspansji, w wyniku której powstaje wiele kopii tego samego limfocytu B, zdolnego do rozpoznania danego antygenu. Wreszcie, te namnożone limfocyty B różnicują się w komórki plazmatyczne, które są wyspecjalizowane w produkcji i wydzielaniu ogromnych ilości przeciwciał. To niezwykle efektywny mechanizm obronny.
Czym są przeciwciała i jak neutralizują zagrożenie na poziomie molekularnym?
Przeciwciała to białka w kształcie litery "Y", które są niezwykle specyficzne dla danego antygenu. Ich działanie jest wielokierunkowe. Mogą neutralizować patogeny, na przykład blokując wirusom możliwość przyłączania się do komórek gospodarza, lub unieszkodliwiając toksyny bakteryjne. Mogą również działać jako "znaczniki" w procesie zwanym opsonizacją, ułatwiając makrofagom i innym komórkom fagocytarnym pochłanianie i niszczenie patogenów. Ponadto, przeciwciała mogą aktywować układ dopełniacza, kaskadę białek, która prowadzi do zniszczenia komórek bakteryjnych. To właśnie te molekularne "pociski" zapewniają nam ochronę przed infekcjami.
Pamięć immunologiczna: fundament długotrwałej ochrony
Kluczowym, a zarazem najbardziej fascynującym elementem odpowiedzi poszczepiennej jest powstawanie pamięci immunologicznej. Nie wszystkie aktywowane limfocyty T i B przekształcają się w komórki efektorowe, które walczą z bieżącą infekcją. Znaczna ich część różnicuje się w długożyjące komórki pamięci limfocyty T pamięci i limfocyty B pamięci. Te "elitarne jednostki" pozostają w organizmie przez wiele lat, a nawet całe życie, stanowiąc swego rodzaju "archiwum" informacji o napotkanych patogenach. To właśnie one są gwarancją szybkiej, silniejszej i skuteczniejszej odpowiedzi wtórnej, gdy ponownie zetkniemy się z tym samym antygenem.
Tworzenie elitarnej jednostki: czym są komórki pamięci T i B?
Komórki pamięci T i B to wyjątkowe limfocyty, które charakteryzują się długowiecznością i gotowością do natychmiastowej reakcji. W przeciwieństwie do komórek efektorowych, które mają krótki czas życia i intensywnie walczą z aktualnym zagrożeniem, komórki pamięci pozostają w stanie spoczynku, ale są niezwykle czujne. Posiadają specyficzne receptory dla antygenu, który je aktywował, i są znacznie liczniejsze niż naiwne limfocyty. Dzięki temu, po ponownej ekspozycji na antygen, mogą błyskawicznie się namnożyć i przekształcić w komórki efektorowe, rozpoczynając obronę.
Dlaczego wtórna odpowiedź immunologiczna jest tak szybka i potężna?
Wtórna odpowiedź immunologiczna jest znacząco szybsza i silniejsza niż pierwotna, co jest bezpośrednim efektem obecności komórek pamięci. Kiedy patogen ponownie wnika do organizmu, komórki pamięci, które już wcześniej spotkały się z tym antygenem, są natychmiast aktywowane. Nie muszą przechodzić przez cały proces pierwotnej aktywacji, co skraca czas reakcji. Ponadto, komórki pamięci namnażają się znacznie intensywniej, produkując większe ilości przeciwciał o wyższym powinowactwie do antygenu. To sprawia, że patogen jest neutralizowany zanim zdąży wywołać chorobę, a my często nawet nie odczuwamy jego obecności.
Na jak długo zapamiętujemy? Różnice w trwałości odporności po różnych szczepieniach
Trwałość pamięci immunologicznej i co za tym idzie, ochrony poszczepiennej, jest zróżnicowana i zależy od wielu czynników, takich jak typ szczepionki, charakterystyka patogenu oraz indywidualne cechy organizmu. Jako Igor Lis, obserwuję, że:
- Niektóre szczepionki, jak np. szczepionka przeciw odrze, śwince i różyczce (MMR), zapewniają odporność, która może utrzymywać się przez całe życie, dzięki silnej i trwałej stymulacji komórek pamięci.
- Inne, takie jak szczepionka przeciw tężcowi, wymagają regularnych dawek przypominających (co 10 lat), aby utrzymać wysoki poziom ochrony.
- W przypadku szczepionki przeciw grypie, konieczne jest coroczne szczepienie, ponieważ wirus grypy mutuje, a pamięć immunologiczna przeciwko konkretnym szczepom nie jest długotrwała.
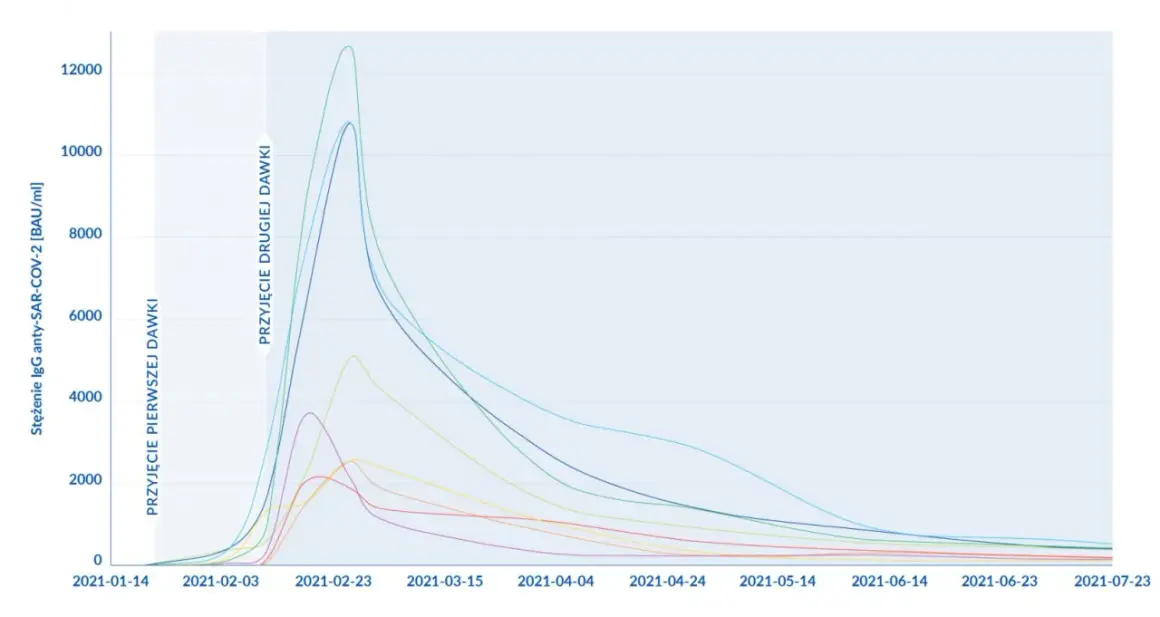
Warto pamiętać, że spadający z czasem poziom przeciwciał we krwi nie zawsze oznacza utratę odporności. Dopóki w organizmie obecne są komórki pamięci, jesteśmy w stanie szybko zareagować na zagrożenie, nawet jeśli poziom krążących przeciwciał jest niski.
Technologie szczepionkowe: różne drogi do tego samego celu
Współczesna medycyna dysponuje różnorodnymi technologiami szczepionkowymi, które, choć różnią się sposobem dostarczania antygenu, mają jeden wspólny cel: efektywną stymulację układu odpornościowego i wytworzenie długotrwałej pamięci immunologicznej. Przyjrzyjmy się kilku kluczowym typom.
Szczepionki mRNA: rewolucyjna instrukcja dla Twoich komórek
Szczepionki mRNA to prawdziwa rewolucja w wakcynologii. Zamiast wprowadzać do organizmu sam antygen, dostarczają one do naszych komórek (najczęściej mięśniowych) fragment informacyjnego RNA (mRNA) z "przepisem" na produkcję białka antygenu, na przykład białka kolca koronawirusa. Komórki organizmu tymczasowo stają się małymi "fabrykami" tych antygenów, produkując je samodzielnie. Te nowo wytworzone białka są następnie rozpoznawane przez układ odpornościowy jako obce, inicjując całą kaskadę odpowiedzi immunologicznej, którą opisałem wcześniej. Skuteczność szczepionek mRNA w stymulowaniu zarówno odporności humoralnej (przeciwciała), jak i komórkowej (limfocyty T) jest wyjątkowo wysoka.
Jak komórka mięśniowa staje się tymczasową "fabryką" antygenów?
Gdy mRNA ze szczepionki dostanie się do cytoplazmy komórki mięśniowej, natychmiast wykorzystuje ono maszynerię komórkową (rybosomy) do translacji, czyli przetłumaczenia genetycznej instrukcji na białko. W ten sposób komórka mięśniowa zaczyna produkować białko antygenu. Część tych białek jest uwalniana na zewnątrz komórki, a część jest prezentowana na jej powierzchni za pośrednictwem cząsteczek MHC. To właśnie te białka i ich fragmenty są następnie rozpoznawane przez komórki prezentujące antygen i limfocyty, co uruchamia odpowiedź immunologiczną. To sprytny sposób na to, by nasz własny organizm "pokazał" układowi odpornościowemu, czego ma się nauczyć.
Dlaczego mRNA jest bezpieczne i nie zmienia naszego DNA?
Kwestia bezpieczeństwa szczepionek mRNA jest często poruszana, dlatego jako Igor Lis, zawsze podkreślam kluczowe fakty. mRNA ze szczepionki nie wnika do jądra komórkowego, gdzie przechowywane jest nasze DNA. Działa wyłącznie w cytoplazmie komórki. Co więcej, mRNA jest cząsteczką krótkotrwałą i po wykonaniu swojej funkcji, czyli po wyprodukowaniu odpowiedniej ilości białka antygenu, ulega naturalnej degradacji przez enzymy komórkowe. Nie ma więc żadnego ryzyka, że mRNA integruje się z naszym DNA lub w jakikolwiek sposób je zmieni. To naturalny proces, który zachodzi w naszych komórkach przez cały czas.
Szczepionki wektorowe: jak "oswojony" wirus dostarcza kluczowe informacje?
Szczepionki wektorowe wykorzystują inną, ale równie pomysłową strategię. W tym przypadku, nieszkodliwy wirus (zwany wektorem, często jest to adenowirus, który został zmodyfikowany tak, aby nie mógł się replikować i wywoływać choroby) służy jako "pojazd" do dostarczenia materiału genetycznego kodującego antygen do naszych komórek. Podobnie jak w przypadku mRNA, nasze komórki same produkują białko antygenu, które następnie stymuluje odpowiedź immunologiczną. Różnica polega na sposobie dostarczania instrukcji: w szczepionkach mRNA jest to bezpośrednie podanie mRNA, natomiast w szczepionkach wektorowych wykorzystanie wirusa jako nośnika DNA, które jest następnie przepisywane na mRNA w komórce.
Przeczytaj również: Jak powstaje mocz? Kluczowe etapy pracy nerek dla Twojego zdrowia
Szczepionki tradycyjne (inaktywowane i podjednostkowe): sprawdzone metody wciąż w grze
Nie możemy zapominać o tradycyjnych technologiach szczepionkowych, które przez dziesięciolecia dowiodły swojej skuteczności i nadal odgrywają ważną rolę. Szczepionki inaktywowane zawierają całe patogeny (np. wirusy), które zostały zabite i nie są w stanie wywołać choroby, ale ich antygeny są nadal obecne i stymulują odporność. Szczepionki podjednostkowe zawierają jedynie oczyszczone fragmenty antygenu (np. białka), które są wystarczające do wywołania odpowiedzi immunologicznej. Mimo że te metody mogą być mniej efektywne w stymulowaniu odporności komórkowej niż szczepionki mRNA czy wektorowe, ich sprawdzona skuteczność i bezpieczeństwo sprawiają, że są nadal cennym narzędziem w profilaktyce chorób zakaźnych.